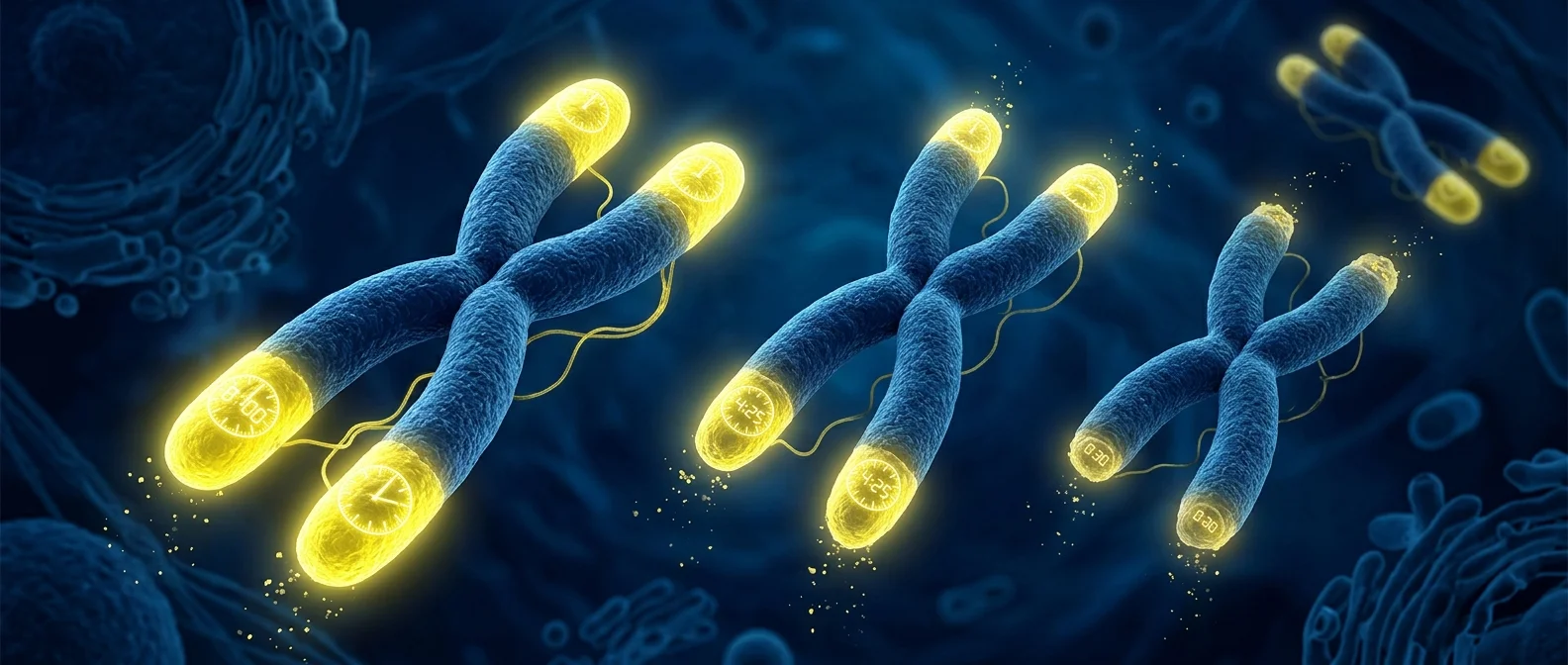
Φαντάσου ότι κάθε κύτταρό σου κουβαλάει ένα αόρατο αντίστροφο χρονόμετρο. Δεν χτυπάει, δεν κάνει θόρυβο — αλλά με κάθε κυτταρική διαίρεση, γίνεται λίγο πιο κοντό. Όταν φτάσει στο μηδέν, το κύτταρο σταματάει να λειτουργεί. Αυτό δεν είναι επιστημονική φαντασία. Είναι η βιολογία των τελομερών, και καθορίζει κυριολεκτικά πόσο γρήγορα γερνάς.
📖 Διαβάστε περισσότερα: 10 Απίστευτα Facts για το Σώμα σου που Δεν Γνώριζες
Τι Ακριβώς Είναι τα Τελομερή;
Στα άκρα κάθε χρωμοσώματος υπάρχουν επαναλαμβανόμενες αλληλουχίες DNA — συγκεκριμένα η ακολουθία TTAGGG, που επαναλαμβάνεται χιλιάδες φορές. Αυτές οι αλληλουχίες δεν κωδικοποιούν κάποιες πρωτεΐνες. Ο ρόλος τους είναι καθαρά προστατευτικός: λειτουργούν σαν τα πλαστικά καπάκια στις άκρες των κορδονιών παπουτσιών. Χωρίς αυτά, τα χρωμοσώματα θα ξεφτίσουν, θα συγκολληθούν μεταξύ τους και θα καταστραφούν κρίσιμα γενετικά δεδομένα. Κατά τη γέννηση, τα τελομερή ενός ανθρώπου έχουν μήκος περίπου 10.000 ζευγαριών βάσεων. Μέχρι τα γηρατειά, αυτό πέφτει κάτω από 4.000. Η φθορά είναι σταδιακή αλλά αμείλικτη — κάθε χρόνο χάνουμε κατά μέσο όρο 20 έως 40 ζεύγη βάσεων ανάλογα με τον τρόπο ζωής μας.
Το Όριο Hayflick: Η Αντίστροφη Μέτρηση
Το 1961, ο Leonard Hayflick ανακάλυψε κάτι που ανέτρεψε δεκαετίες πεποιθήσεων. Τα ανθρώπινα κύτταρα δεν μπορούν να διαιρεθούν απεριόριστα — υπάρχει ένα αυστηρό ανώτατο όριο. Συγκεκριμένα, τα περισσότερα σωματικά κύτταρα μπορούν να πραγματοποιήσουν μόνο 50 έως 70 διαιρέσεις πριν σταματήσουν οριστικά. Ο λόγος; Με κάθε αντιγραφή DNA, η DNA πολυμεράση αδυνατεί να αντιγράψει πλήρως τα άκρα του χρωμοσώματος. Έτσι χάνονται 50 με 200 ζεύγη βάσεων κάθε φορά. Οι πρώτες δεκάδες διαιρέσεις «τρώνε» μόνο τελομερικό DNA — δηλαδή αναλώσιμο υλικό. Αλλά μόλις εξαντληθεί αυτό το απόθεμα, η φθορά αρχίζει να πλήττει γονίδια ζωτικής σημασίας. Η αρχή του «τέλους» για ένα κύτταρο δεν μοιάζει με δραματική κατάρρευση — μοιάζει με αργή σιωπηλή εξάντληση. Τα πρώτα σημάδια εμφανίζονται ως αδυναμία του κυττάρου να αποκρίνεται σε αυξητικά σήματα.

Η Shelterin: Ομάδα Σωματοφυλάκων του DNA
Τα τελομερή δεν είναι μόνα τους. Μια ομάδα έξι πρωτεϊνών, γνωστή ως σύμπλεγμα shelterin, τα περιβάλλει και τα σταθεροποιεί. Οι πρωτεΐνες TRF1, TRF2, POT1, TIN2, TPP1 και RAP1 συνεργάζονται για να κρύψουν τα άκρα των χρωμοσωμάτων από τους μηχανισμούς επιδιόρθωσης DNA. Γιατί αυτό είναι σημαντικό; Γιατί χωρίς τη shelterin, το κύτταρο θα αντιλαμβανόταν τα ελεύθερα άκρα ως σπασμένο DNA και θα ενεργοποιούσε μηχανισμούς απόπτωσης. Ουσιαστικά, η shelterin «εξαπατά» το κύτταρο, κάνοντάς το να πιστεύει ότι όλα πάνε καλά — μέχρι τα τελομερή γίνουν τόσο κοντά που δεν μπορούν πλέον να κρυφτούν. Σε αυτό το σημείο, ενεργοποιούνται οι πρωτεΐνες p53 και pRb, οι κύριοι «φρουροί» του κυτταρικού κύκλου, και σταματούν κάθε περαιτέρω διαίρεση. Η ισορροπία μεταξύ προστασίας shelterin και πρωτεϊνικής αντίδρασης καθορίζει αν ένα κύτταρο θα ζήσει ή θα μπει σε γήρανση.
Τελομεράση: Το Ένζυμο της «Αθανασίας»
Υπάρχει ένα ένζυμο που μπορεί να αντιστρέψει τη βράχυνση των τελομερών. Λέγεται τελομεράση, και ανακαλύφθηκε το 1984 από την Elizabeth Blackburn και την Carol Greider μελετώντας το μονοκύτταρο πρωτόζωο Tetrahymena thermophila. Η τελομεράση προσθέτει αλληλουχίες TTAGGG στα άκρα των χρωμοσωμάτων, αντισταθμίζοντας τη φυσιολογική φθορά. Το πρόβλημα; Στα περισσότερα σωματικά κύτταρα ενός ενήλικα η τελομεράση είναι απενεργοποιημένη. Παραμένει ενεργή μόνο στα βλαστοκύτταρα, στα αναπαραγωγικά κύτταρα και σε ορισμένα κύτταρα του ανοσοποιητικού. Αυτή η ανακάλυψη χάρισε στους Blackburn, Greider και Jack Szostak το Νόμπελ Φυσιολογίας και Ιατρικής το 2009. Η τελομεράση ανήκει σε μια ιδιαίτερη κατηγορία ενζύμων — τις αντίστροφες μεταγραφάσες — γιατί χρησιμοποιεί ένα RNA πρότυπο για να κατασκευάσει DNA. Κάθε φορά που δρα, δημιουργεί ένα μικρό κομμάτι νέου τελομερικού DNA, αναπληρώνοντας αυτό που χάθηκε.
Καρκίνος: Όταν το Ρολόι Σταματάει να Μετράει
Αν η τελομεράση μπορεί να αναγεννήσει τα τελομερή, γιατί δεν την ενεργοποιούμε παντού; Η απάντηση κρύβει έναν παράδοξο κίνδυνο. Περίπου στο 85-90% όλων των καρκίνων, τα καρκινικά κύτταρα έχουν επανενεργοποιήσει την τελομεράση. Αυτό τους επιτρέπει να διαιρούνται απεριόριστα — ξεπερνώντας το όριο Hayflick και γινόμενα ουσιαστικά αθάνατα. Τα κύτταρα HeLa, που προέρχονται από την Henrietta Lacks το 1951, συνεχίζουν να πολλαπλασιάζονται σε εργαστήρια σε όλο τον κόσμο ακριβώς επειδή η τελομεράσή τους δεν σβήνει ποτέ. Αυτό σημαίνει ότι η τελομεράση είναι ταυτόχρονα η ελπίδα και ο εφιάλτης της κυτταρικής βιολογίας — ένα μαχαίρι που κόβει και από τις δύο πλευρές. Ερευνητικά εργαστήρια σε όλο τον κόσμο αναζητούν τρόπους να ελέγξουν εκλεκτικά την τελομεράση: να την ενεργοποιούν στα υγιή κύτταρα ενώ την αποσιωπούν στα καρκινικά. Μέχρι στιγμής, η πρόκληση παραμένει τεράστια.

Στρες, Τραύμα και Η Φθορά που Δεν Βλέπεις
Το 2004, μια δημοσίευση στο Proceedings of the National Academy of Sciences από τις Elissa Epel και Elizabeth Blackburn άλλαξε τον τρόπο που βλέπουμε τη σχέση ψυχολογίας και γήρανσης. Μελέτησαν μητέρες που φρόντιζαν χρόνια άρρωστα παιδιά και ανακάλυψαν κάτι εντυπωσιακό: όσο περισσότερα χρόνια φροντίδας είχαν οι μητέρες, τόσο πιο μικρά ήταν τα τελομερή τους. Η διαφορά ήταν ισοδύναμη με 9 έως 17 χρόνια επιπλέον βιολογικής γήρανσης. Και το πιο συγκλονιστικό: η χρονολογική ηλικία δεν προέβλεπε το μήκος των τελομερών — αλλά το επίπεδο στρες προέβλεπε. Η κορτιζόλη, η βασική ορμόνη του χρόνιου στρες, αυξάνει δραματικά τον οξειδωτικό φόρτο στα κύτταρα και επιταχύνει τη βράχυνση των τελομερών. Το χρόνιο καθημερινό στρες κυριολεκτικά σε γερνάει σταδιακά από μέσα.
Μπορείς να Επιβραδύνεις τα Ρολόγια;
Η καλή είδηση είναι ότι ο ρυθμός βράχυνσης δεν είναι σταθερός — επηρεάζεται σημαντικά από τον τρόπο ζωής. Η αερόβια άσκηση αυξάνει τα επίπεδα τελομεράσης στα λευκά αιμοσφαίρια. Μια μελέτη του Werner et al. (2009) στο περιοδικό Circulation έδειξε ότι δρομείς μεγάλων αποστάσεων είχαν σημαντικά μακρύτερα τελομερή σε σύγκριση με καθιστικά άτομα ίδιας ηλικίας. Η Μεσογειακή διατροφή, πλούσια σε αντιοξειδωτικά, ωμέγα-3 λιπαρά οξέα και φυτικές ίνες, συνδέεται επίσης με πιο αργό ρυθμό φθοράς. Ακόμη και ο διαλογισμός φαίνεται να βοηθάει: μια μελέτη της Lavretsky et al. δημοσιευμένη στο International Journal of Geriatric Psychiatry βρήκε ότι εντατικός διαλογισμός για μόλις 12 λεπτά ημερησίως αύξησε τη δραστηριότητα τελομεράσης κατά 43% μέσα σε δύο μήνες. Ο ύπνος παίζει επίσης ρόλο: λιγότερες από 6 ώρες τη νύχτα συνδέονται επανειλημμένα με βραχύτερα τελομερή σε πολλαπλές πληθυσμιακές μελέτες.
Παράγοντες που Επηρεάζουν τα Τελομερή
Θετικοί: Αερόβια άσκηση, Μεσογειακή διατροφή, διαλογισμός, κοινωνικές σχέσεις, επαρκής ύπνος, αντιοξειδωτικά (βιταμίνη C, βιταμίνη E)
Αρνητικοί: Χρόνιο στρες, κάπνισμα, παχυσαρκία, αϋπνία, ζάχαρη, κατάθλιψη, κατανάλωση αλκοόλ, φλεγμονή
Γηρασμένα Κύτταρα: Οι Ζόμπι του Σώματος
Όταν τα τελομερή φτάσουν σε κρίσιμα χαμηλό μήκος, το κύτταρο εισέρχεται σε κατάσταση κυτταρικής γήρανσης (senescence). Δεν πεθαίνει, αλλά σταματάει να διαιρείται. Αυτό ακούγεται αβλαβές, αλλά δεν είναι: τα γηρασμένα κύτταρα εκκρίνουν ένα μείγμα φλεγμονωδών μορίων γνωστό ως SASP (Senescence-Associated Secretory Phenotype). Αυτές οι ενώσεις — ιντερλευκίνες, μεταλλοπρωτεΐνες και χημειοκίνες — βλάπτουν τα γειτονικά υγιή κύτταρα και τροφοδοτούν χρόνια φλεγμονή. Τα γηρασμένα κύτταρα συσσωρεύονται με την ηλικία και ενοχοποιούνται για νόσους όπως αρθρίτιδα, αθηροσκλήρωση και νευροεκφυλιστικές παθήσεις. Φαρμακευτικοί παράγοντες λεγόμενοι σενολυτικά στοχεύουν πλέον στην εκλεκτική εξάλειψη αυτών των κυττάρων-ζόμπι. Σε πειράματα με ποντίκια, η χορήγηση σενολυτικών ουσιών όπως η κομπινασιόν dasatinib και quercetin βελτίωσε τη σωματική αντοχή, μείωσε τη φλεγμονή και αύξησε τη μέση διάρκεια ζωής. Κλινικές δοκιμές σε ανθρώπους βρίσκονται ήδη σε εξέλιξη.
«Τα τελομερή δεν καθορίζουν μόνο πόσο θα ζήσεις — καθορίζουν πώς θα γεράσεις.»
— Elizabeth Blackburn, Νομπελίστρια Φυσιολογίας 2009Πηγές:
- Blackburn, E.H., Greider, C.W. & Szostak, J.W. — «Telomeres and telomerase: the path from maize, Tetrahymena and yeast to human cancer and aging», Nature Medicine, 2006
- Epel, E.S. et al. — «Accelerated telomere shortening in response to life stress», Proceedings of the National Academy of Sciences, 2004