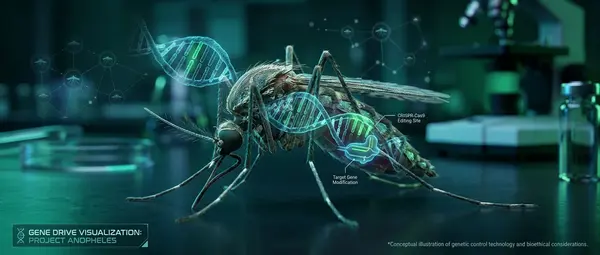
Τον Νοέμβριο του 2018, ένας Κινέζος ερευνητής ανακοίνωσε ότι δύο κοριτσάκια — η Λούλου και η Νάνα — γεννήθηκαν με γονίδια τροποποιημένα μέσω CRISPR, προκαλώντας παγκόσμια κατακραυγή. Ταυτόχρονα, μια εντελώς διαφορετική πλευρά της ίδιας τεχνολογίας θεράπευε ασθενείς με δρεπανοκυτταρική αναιμία για πρώτη φορά στην ιστορία. Το CRISPR-Cas9 είναι ταυτόχρονα η πιο ελπιδοφόρα και η πιο αμφιλεγόμενη ανακάλυψη της σύγχρονης γενετικής — ένα μοριακό «ψαλίδι» που μπορεί να κόψει, να διορθώσει ή να ξαναγράψει τον κώδικα της ζωής.
📖 Διαβάστε περισσότερα: 80% του DNA σου Δεν Κάνει Τίποτα; Ή Μήπως Κάνει;
Τι Είναι το CRISPR: Το Μοριακό Ψαλίδι
Το CRISPR (Clustered Regularly Interspaced Short Palindromic Repeats) είναι ένα φυσικό ανοσοποιητικό σύστημα των βακτηρίων. Όταν ένας ιός μολύνει ένα βακτήριο και αυτό επιβιώνει, αποθηκεύει ένα κομμάτι του ιικού DNA στο δικό του γονιδίωμα — σαν «αστυνομικό αρχείο». Αν ο ίδιος ιός επιτεθεί ξανά, το βακτήριο χρησιμοποιεί αυτό το αρχείο για να κατευθύνει την πρωτεΐνη Cas9, η οποία κόβει το DNA του εισβολέα σε συγκεκριμένο σημείο.
Οι Jennifer Doudna (UC Berkeley) και Emmanuelle Charpentier (Ινστιτούτο Max Planck) συνειδητοποίησαν ότι αυτός ο βακτηριακός αμυντικός μηχανισμός μπορεί να μετατραπεί σε πανίσχυρο εργαλείο γενετικής επεξεργασίας. Το 2012 δημοσίευσαν στο Science ότι κατασκεύασαν ένα συνθετικό «οδηγό RNA» (guide RNA) που κατευθύνει την Cas9 σε οποιοδήποτε σημείο του γονιδιώματος με ακρίβεια λίγων νουκλεοτιδίων. Η πρωτεΐνη κόβει και τις δύο αλυσίδες του DNA, και μετά η κυτταρική μηχανή επισκευάζει το σπάσιμο — είτε απλά κολλώντας τις άκρες (NHEJ), είτε χρησιμοποιώντας ένα «πρότυπο» που δίνουν οι ερευνητές (HDR). Το 2020 τιμήθηκαν με Νόμπελ Χημείας.

Η Υπόθεση He Jiankui: Τα Πρώτα «Σχεδιασμένα» Μωρά
Τον Νοέμβριο του 2018, ο He Jiankui από το Νότιο Πανεπιστήμιο Επιστήμης και Τεχνολογίας της Σενζέν ανακοίνωσε ότι τροποποίησε γενετικά ανθρώπινα έμβρυα εξωσωματικής γονιμοποίησης, απενεργοποιώντας το γονίδιο CCR5 — έναν υποδοχέα που χρησιμοποιεί ο HIV για να εισβάλει στα κύτταρα. Τα δύο κοριτσάκια γεννήθηκαν φαινομενικά υγιή, αλλά η αντίδραση της επιστημονικής κοινότητας ήταν σαρωτική.
Πάνω από 120 Κινέζοι επιστήμονες υπέγραψαν ανοιχτή επιστολή καταδίκης. Ο He Jiankui καταδικάστηκε σε 3 χρόνια φυλάκιση και πρόστιμο 3 εκατομμυρίων γιουάν. Το πρόβλημα δεν ήταν μόνο ηθικό: η τροποποίηση του CCR5 ήταν μωσαϊκή (δεν πέτυχε σε όλα τα κύτταρα), δεν υπήρχε πραγματική ιατρική ανάγκη (ο πατέρας ήταν HIV-θετικός, αλλά υπάρχουν ασφαλέστερες μέθοδοι πρόληψης), και αυτή η αλλαγή κληρονομείται στις επόμενες γενιές — μια απόφαση που πάρθηκε χωρίς τη συγκατάθεση αυτών που θα επηρεαστούν.
Χρωμοσώματα που Εξαφανίζονται: Η Μελέτη της Columbia
Σε μελέτη του 2020 στο Cell, επιστήμονες του Columbia ανακάλυψαν ότι η χρήση CRISPR σε ανθρώπινα έμβρυα μπορεί να προκαλέσει απώλεια ολόκληρου χρωμοσώματος — ένα αποτέλεσμα πολύ πιο σοβαρό από τις αναμενόμενες μικρές αλλαγές.
Ο Dieter Egli και η ομάδα του στο Columbia University δοκίμασαν το CRISPR σε ανθρώπινα έμβρυα που έφεραν μετάλλαξη στο γονίδιο EYS, υπεύθυνο για κληρονομική τύφλωση. Αντί για ακριβή διόρθωση, ανακάλυψαν ένα τρίτο, απρόσμενο αποτέλεσμα: η κοπή του DNA οδηγούσε συχνά σε απώλεια ολόκληρου χρωμοσώματος ή μεγάλου τμήματος αυτού.
«Μάθαμε ότι στα ανθρώπινα εμβρυϊκά κύτταρα, ένα μόνο σπάσιμο στο DNA μπορεί να οδηγήσει σε απώλεια ολόκληρου χρωμοσώματος, και αυτή η απώλεια είναι πολύ συχνή», εξήγησε ο Michael Zuccaro, συν-πρωτοσυγγραφέας της μελέτης. Η ομάδα αναθεώρησε ακόμα και τα αποτελέσματα παλαιότερης μελέτης του 2017 που είχε αναφέρει «επιτυχή διόρθωση» καρδιακής μετάλλαξης: πιθανολόγησε ότι αντί για διόρθωση, το χρωμόσωμα με τη μετάλλαξη είχε απλώς χαθεί ολόκληρο. «Αν τα αποτελέσματά μας ήταν γνωστά δύο χρόνια πριν, αμφιβάλλω αν κάποιος θα προχωρούσε», σχολίασε ο Egli.
Η Πρώτη Εγκεκριμένη Θεραπεία: CASGEVY και Δρεπανοκυτταρική
Τον Δεκέμβριο του 2023, ο FDA ενέκρινε το CASGEVY (exagamglogene autotemcel) — την πρώτη θεραπεία βασισμένη σε CRISPR — για τη δρεπανοκυτταρική αναιμία και τη β-θαλασσαιμία. Πρόκειται για θεραπεία ex vivo: τα αιμοποιητικά βλαστοκύτταρα αφαιρούνται από τον ασθενή, τροποποιούνται με CRISPR ώστε να παράγουν εμβρυϊκή αιμοσφαιρίνη (HbF) αντί της ελαττωματικής HbS, και επανεγχέονται στον οργανισμό.
Η δρεπανοκυτταρική αναιμία προκαλείται από μια μοναδική μετάλλαξη στο γονίδιο HBB, που κάνει τα ερυθρά αιμοσφαίρια να παραμορφώνονται σε σχήμα δρεπανιού, προκαλώντας χρόνιο πόνο, αναιμία και βλάβη οργάνων. Περίπου 100.000 Αμερικανοί πάσχουν από τη νόσο. Το CASGEVY «ξυπνά» ένα γονίδιο που φυσιολογικά σβήνει μετά τη γέννηση, παράγοντας εμβρυϊκή αιμοσφαιρίνη που αντικαθιστά λειτουργικά την ελαττωματική.

In Vivo CRISPR: Η Θεραπεία Μέσα στο Σώμα
Το επόμενο βήμα είναι η in vivo θεραπεία — γονιδιακή επεξεργασία απευθείας μέσα στον οργανισμό. Σύμφωνα με μελέτη δημοσιευμένη στο New England Journal of Medicine τον Φεβρουάριο 2024, η θεραπεία NTLA-2002 της Intellia Therapeutics χρησιμοποιεί CRISPR/Cas9 για να τροποποιήσει το γονίδιο KLKB1 απευθείας στο ήπαρ ασθενών με κληρονομικό αγγειοοίδημα — μια σπάνια γενετική διαταραχή (1 στους 50.000) που προκαλεί επικίνδυνα τα οιδήματα.
Η Hilary Longhurst από το Πανεπιστήμιο του Auckland, επικεφαλής της έρευνας, ανέφερε ότι μια μοναδική ενδοφλέβια έγχυση μείωσε τα επίπεδα πλασματικής καλλικρεΐνης κατά 95% και τις κρίσεις οιδήματος κατά 95%. Οι ασθενείς σταμάτησαν τα φάρμακά τους και θα παρακολουθούνται για 15 χρόνια. Σε αντίθεση με το CASGEVY, εδώ η επεξεργασία γίνεται μέσα στο σώμα — ένα σημαντικό βήμα προς πιο προσιτές θεραπείες χωρίς μεταμόσχευση.
Base Editing και Prime Editing: Η Επόμενη Γενιά
Το κλασικό CRISPR κόβει και τις δύο αλυσίδες του DNA, δημιουργώντας κίνδυνο ανεπιθύμητων αλλαγών. Γι' αυτό αναπτύχθηκαν νέες, ακριβέστερες τεχνικές. Το base editing, που εφευρέθηκε από τον David Liu στο Broad Institute το 2016, αλλάζει ένα μεμονωμένο «γράμμα» DNA (π.χ. C→T ή A→G) χωρίς να κόψει τη διπλή έλικα — σαν να αλλάζεις ένα γράμμα σε μια λέξη αντί να ξαναγράφεις ολόκληρη τη σελίδα.
Το prime editing (2019, επίσης David Liu) πάει ακόμα παραπέρα: μπορεί να εισάγει, να διαγράψει ή να αντικαταστήσει μικρές αλληλουχίες DNA χωρίς διπλό σπάσιμο και χωρίς εξωτερικό πρότυπο DNA. Θεωρείται ότι μπορεί να διορθώσει έως και το 89% των γνωστών παθογόνων μεταλλάξεων. Μια ακόμα πιο πρόσφατη εξέλιξη, το epigenome editing, αλλάζει τη γονιδιακή έκφραση χωρίς καν να τροποποιήσει την αλληλουχία — «ανοίγει» ή «κλείνει» γονίδια χωρίς μόνιμη αλλαγή στον κώδικα.
Σχεδιασμένα Μωρά: Πού Βρίσκεται η Κόκκινη Γραμμή;
Η διάκριση-κλειδί είναι μεταξύ σωματικής (somatic) και γαμετικής (germline) επεξεργασίας. Οι σωματικές θεραπείες όπως το CASGEVY επηρεάζουν μόνο τον ασθενή — δεν κληρονομούνται. Η γαμετική επεξεργασία, αντίθετα, αλλάζει τα ωάρια, τα σπερματοζωάρια ή τα έμβρυα, επηρεάζοντας κάθε γενιά στο μέλλον. Σήμερα, πάνω από 70 χώρες απαγορεύουν ή ρυθμίζουν αυστηρά την γαμετική επεξεργασία ανθρώπινων εμβρύων.
Η μελέτη Selmecki et al. του 2019 έδειξε ότι ακόμα και η «επιλογή εμβρύων» βάσει πολυγονιδιακών χαρακτηριστικών (ύψος, νοημοσύνη) δεν μπορεί να προβλέψει αξιόπιστα. Ένα ζευγάρι που θα ήθελε το ψηλότερο παιδί θα κέρδιζε στατιστικά μόλις 2,5 εκατοστά — ενώ τα περιβαλλοντικά αποτελέσματα κυριαρχούν. Η αποφυγή μονογονιδιακών ασθενειών (Huntington, κυστική ίνωση) μέσω PGD είναι ήδη καθιερωμένη πρακτική — αλλά η «βελτίωση» υγιών εμβρύων παραμένει ηθικά και τεχνικά στον κόσμο της επιστημονικής φαντασίας.
Μέχρι σήμερα, περισσότερα από 50 κλινικά πρωτόκολλα βασισμένα σε CRISPR βρίσκονται σε εξέλιξη παγκοσμίως, στοχεύοντας καρκίνο, HIV, τύφλωση, μυϊκή δυστροφία, β-θαλασσαιμία και δεκάδες σπάνιες γενετικές νόσους.
Το Μέλλον: Θεραπεία ή Σχεδιασμός;
Η τεχνολογία CRISPR εξελίσσεται ταχύτατα. Νέα συστήματα όπως το CasΦ (ανακαλύφθηκε σε βακτηριοφάγους και είναι κατά 50% μικρότερο), το Cas12 και το Cas13 (που στοχεύει RNA αντί DNA) διευρύνουν τις δυνατότητες. Η τεχνολογία λιπιδικών νανοσωματιδίων (LNP), η ίδια που χρησιμοποιήθηκε στα εμβόλια mRNA, καθιστά πλέον δυνατή τη μεταφορά CRISPR σε συγκεκριμένα όργανα χωρίς ιικούς φορείς.
Η μεγάλη ερώτηση δεν είναι πια «μπορούμε;» αλλά «πρέπει;». Η θεραπεία γενετικών ασθενειών είναι ηθικά θεμιτή και ιατρικά επαναστατική — κανείς δεν αμφισβητεί ότι η εξάλειψη της δρεπανοκυτταρικής ή της κυστικής ίνωσης θα ήταν νίκη της ανθρωπότητας. Η «βελτίωση» υγιών ανθρώπων — αυξημένη μυϊκή μάζα, αντοχή σε ασθένειες, ακόμα και διανοητική ενίσχυση — ανοίγει ένα κουτί της Πανδώρας. Όπως δήλωσε ο Egli μετά τη μελέτη του: «Η ελπίδα μας είναι ότι αυτά τα αποτελέσματα θα αποθαρρύνουν πρόωρη κλινική εφαρμογή, αλλά θα κατευθύνουν επίσης υπεύθυνη έρευνα για ασφαλή και αποτελεσματική χρήση».
Πηγές:
- Zuccaro, M.V. et al. «Allele-specific chromosome removal after Cas9 cleavage in human embryos.» Cell, 2020 — ScienceDaily, Columbia University Irving Medical Center
- Longhurst, H.J. et al. «CRISPR-Cas9 In Vivo Gene Editing of KLKB1 for Hereditary Angioedema.» New England Journal of Medicine, 2024 — ScienceDaily, University of Auckland