Κάθε χρόνο, ανθεκτικά βακτήρια σκοτώνουν πάνω από 1,2 εκατομμύρια ανθρώπους παγκοσμίως — και ο αριθμός αυξάνεται. Τα αντιβιοτικά, κάποτε ο θρίαμβος της σύγχρονης ιατρικής, χάνουν σταδιακά τη δύναμή τους. Μια ομάδα βιολόγων στο Πανεπιστήμιο της Καλιφόρνια, Σαν Ντιέγκο, μόλις αποκάλυψε ένα εργαλείο που δεν στοχεύει τα βακτήρια — στοχεύει τα ίδια τα γονίδια που τα κάνουν ανθεκτικά.
📖 Διαβάστε ακόμα: Βακτήρια 5.000 Ετών Αντέχουν Σύγχρονα Αντιβιοτικά
🧬 Τι Είναι η Αντίσταση στα Αντιβιοτικά και Γιατί Μας Τρομάζει
Η αντίσταση στα αντιβιοτικά (Antimicrobial Resistance — AMR) δεν είναι μελλοντικό σενάριο. Είναι ήδη εδώ. Βακτήρια που κάποτε αντιμετωπίζονταν εύκολα με πενικιλίνη ή αμοξικιλλίνη, σήμερα απαιτούν «αντιβιοτικά τελευταίας γραμμής» — και ακόμη και αυτά αρχίζουν να αποτυγχάνουν. Σύμφωνα με εκτιμήσεις, αν δεν αλλάξει κάτι ριζικά, τα ανθεκτικά «superbug» βακτήρια θα σκοτώνουν πάνω από 10 εκατομμύρια ανθρώπους κάθε χρόνο μέχρι το 2050.
Τα βακτήρια αναπτύσσουν αντίσταση με πολλούς τρόπους. Ο πιο ανησυχητικός είναι μέσω πλασμιδίων — κυκλικών τμημάτων DNA που αναπαράγονται μέσα σε κύτταρα και μεταφέρουν γονίδια αντοχής από βακτήριο σε βακτήριο. Αυτό σημαίνει ότι η αντίσταση εξαπλώνεται ακόμα και χωρίς κληρονομικότητα — σαν μεταδοτική ασθένεια ανάμεσα σε μικρόβια.
🔬 Η Νέα Τεχνολογία: pPro-MobV — Ένα «Gene Drive» για Βακτήρια
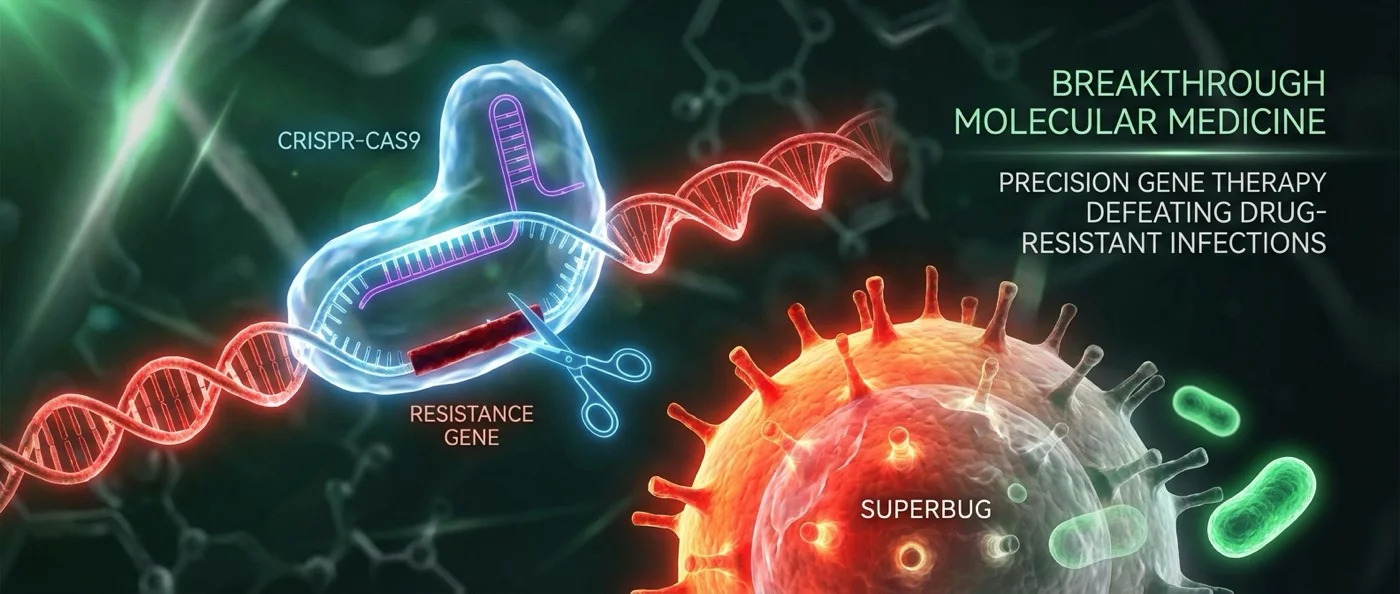
Η ομάδα των καθηγητών Ethan Bier και Justin Meyer στο UC San Diego ανέπτυξε ένα σύστημα βασισμένο στο CRISPR που λειτουργεί σαν «gene drive» — αλλά αντί να στοχεύει έντομα, στοχεύει βακτήρια. Το εργαλείο ονομάζεται pPro-MobV και αποτελεί δεύτερη γενιά της τεχνολογίας Pro-Active Genetics (Pro-AG) που είχε αναπτυχθεί αρχικά το 2019 σε συνεργασία με τον καθηγητή Victor Nizet.
Η βασική αρχή λειτουργίας: ένα γενετικό «κασέτα» CRISPR εισάγεται σε μερικά βακτήρια. Εκεί, η κασέτα κόβει ακριβώς τα γονίδια αντίστασης στα αντιβιοτικά που βρίσκονται πάνω στα πλασμίδια. Αλλά το κλειδί δεν είναι μόνο αυτό — η κασέτα στη συνέχεια αντιγράφεται και εξαπλώνεται σε γειτονικά βακτήρια μέσω συζυγίας (conjugal transfer), ένα είδος «ζευγαρώματος» στον βακτηριακό κόσμο.
«Με το pPro-MobV μεταφέραμε τη λογική του gene drive από τα έντομα στα βακτήρια, ως εργαλείο μηχανικής πληθυσμών. Με αυτήν τη νέα τεχνολογία CRISPR μπορούμε να πάρουμε λίγα κύτταρα και να τα αφήσουμε να εξουδετερώσουν την αντίσταση σε ολόκληρο πληθυσμό.»
— Ethan Bier, Καθηγητής Κυτταρικής και Αναπτυξιακής Βιολογίας, UC San Diego🦠 Πώς Λειτουργεί: Από Κύτταρο σε Κύτταρο
Η πρώτη γενιά Pro-AG (2019) μπορούσε να εισάγει τη γενετική κασέτα μέσα σε βακτήρια, αλλά η εξάπλωσή της ήταν περιορισμένη. Το νέο pPro-MobV εκμεταλλεύεται ένα φαινόμενο που ονομάζεται «σήραγγα σύζευξης» — ένα φυσικό κανάλι που δημιουργούν τα βακτήρια για να ανταλλάσσουν γενετικό υλικό. Μέσω αυτής, τα στοιχεία CRISPR μεταφέρονται αυτόματα από ένα κύτταρο-δότη στα γειτονικά βακτήρια, δημιουργώντας ένα αλυσιδωτό αποτέλεσμα.
Η ομάδα απέδειξε ότι το σύστημα λειτουργεί ακόμα και μέσα σε βιοφίλμ — αποικίες μικροοργανισμών που σχηματίζουν ένα προστατευτικό στρώμα πάνω σε επιφάνειες. Τα βιοφίλμ θεωρούνται εφιάλτης στην κλινική πρακτική: τα αντιβιοτικά δυσκολεύονται να περάσουν μέσα σε αυτά, και η πλειονότητα σοβαρών λοιμώξεων στα νοσοκομεία σχετίζεται με βιοφίλμ. Η δυνατότητα του pPro-MobV να δρα εντός αυτών είναι κρίσιμη.
💡 Η Διαφορά με τα Κλασικά Αντιβιοτικά
Τα παραδοσιακά αντιβιοτικά σκοτώνουν βακτήρια — αλλά δημιουργούν εξελικτική πίεση που ευνοεί τα πιο ανθεκτικά. Το pPro-MobV δεν σκοτώνει κανένα βακτήριο. Αντ' αυτού, αφαιρεί τα «όπλα» τους — τα γονίδια αντοχής — ώστε τα κλασικά αντιβιοτικά να ξαναγίνουν αποτελεσματικά.
📖 Διαβάστε ακόμα: Μικροπλαστικά στο Μοναδικό Έντομο της Ανταρκτικής
🧪 Βακτηριοφάγοι ως Σύμμαχοι
Οι ερευνητές πήγαν ένα βήμα παραπέρα: ανακάλυψαν ότι τα στοιχεία του pPro-MobV μπορούν να μεταφερθούν και μέσω βακτηριοφάγων — ιών που μολύνουν αποκλειστικά βακτήρια. Οι βακτηριοφάγοι (ή «φάγοι») είναι φυσικοί εχθροί των βακτηρίων και ήδη μελετώνται εντατικά ως εναλλακτική θεραπεία στη μετα-αντιβιοτική εποχή. Η ιδέα είναι να χρησιμοποιηθούν μηχανισμοί φάγων σε συνδυασμό με το pPro-MobV, δημιουργώντας ένα ισχυρό «δίδυμο» που εισβάλλει στα βακτήρια, παρακάμπτει τις άμυνές τους, και αδρανοποιεί τα γονίδια αντίστασης.
🏥 Πού Μπορεί να Εφαρμοστεί
Οι εφαρμογές της τεχνολογίας εκτείνονται πολύ πέρα από τα νοσοκομεία. Η αντίσταση στα αντιβιοτικά ευδοκιμεί σε νοσοκομειακά περιβάλλοντα, μονάδες επεξεργασίας λυμάτων, ιχθυοτροφεία και εκτροφεία ζώων. Σε αυτά τα περιβάλλοντα, τα βακτήρια σχηματίζουν πυκνά βιοφίλμ σε σωλήνες, δεξαμενές και εξοπλισμό — ιδανικό πεδίο δράσης για τη νέα τεχνολογία.
«Αν μπορούσαμε να μειώσουμε τη μετάδοση αντίστασης από τα ζώα στους ανθρώπους, θα μπορούσαμε να επηρεάσουμε σημαντικά το πρόβλημα, καθώς περίπου τα μισά ανθεκτικά στελέχη εκτιμάται ότι προέρχονται από το περιβάλλον.»
— Ethan Bier, UC San Diego📖 Διαβάστε ακόμα: Μικροσκόπιο Κβαντικής Εποχής Μετρά 4 Ιδιότητες Μαζί
🔒 Μηχανισμός Ασφαλείας
Ένα εύλογο ερώτημα: τι γίνεται αν η γενετική κασέτα ξεφύγει χωρίς έλεγχο; Η ομάδα ενσωμάτωσε μηχανισμό ασφαλείας βασισμένο σε «ομολογική διαγραφή» (homology-based deletion). Αυτή η τεχνική επιτρέπει την απομάκρυνση της κασέτας CRISPR αν αυτό κριθεί απαραίτητο, λειτουργώντας σαν «διακόπτης απενεργοποίησης» για ολόκληρο το σύστημα.
«Αυτή η τεχνολογία είναι ένας από τους λίγους τρόπους που γνωρίζω ότι μπορεί ενεργά να αντιστρέψει τη διασπορά γονιδίων αντίστασης στα αντιβιοτικά, αντί απλώς να επιβραδύνει ή να αντιμετωπίζει την εξάπλωσή τους.»
— Justin Meyer, Καθηγητής Οικολογίας, Συμπεριφοράς και Εξέλιξης, UC San Diego⚡ Τι Σημαίνει Αυτό για το Μέλλον
Η δημοσίευση στο npj Antimicrobials and Resistance (περιοδικό Nature) σηματοδοτεί ένα σημαντικό βήμα. Ωστόσο, πρόκειται ακόμη για εργαστηριακή έρευνα — η κλινική εφαρμογή απαιτεί πολλά ακόμα χρόνια δοκιμών. Παρ' όλα αυτά, η αρχή λειτουργίας του pPro-MobV αλλάζει τη λογική: αντί να ψάχνουμε συνεχώς νέα αντιβιοτικά στον αγώνα δρόμου με τα βακτήρια, αφοπλίζουμε την ίδια την αντίσταση.
Η τεχνολογία ανοίγει δρόμους σε τρεις κατευθύνσεις: κλινική ιατρική (καταπολέμηση νοσοκομειακών λοιμώξεων), περιβαλλοντική αποκατάσταση (καθαρισμός μολυσμένων υδάτων και εδαφών), και μηχανική μικροβιώματος (επαναπρογραμματισμός βακτηριακών πληθυσμών). Αν τα κλινικά αποτελέσματα επιβεβαιώσουν τις εργαστηριακές υποσχέσεις, θα πρόκειται για αλλαγή παραδείγματος στην αντιμετώπιση μιας από τις μεγαλύτερες υγειονομικές κρίσεις του 21ου αιώνα.
Πηγές: