Φανταστείτε ένα μικροσκοπικό «ψαλίδι» που κόβει το DNA στο ακριβές σημείο, αφαιρεί ένα ελαττωματικό γονίδιο και το αντικαθιστά με υγιές. Δεν είναι επιστημονική φαντασία — είναι η τεχνολογία CRISPR-Cas9, που ήδη θεραπεύει ασθένειες που θεωρούνταν ανίατες.
Τι Είναι το CRISPR
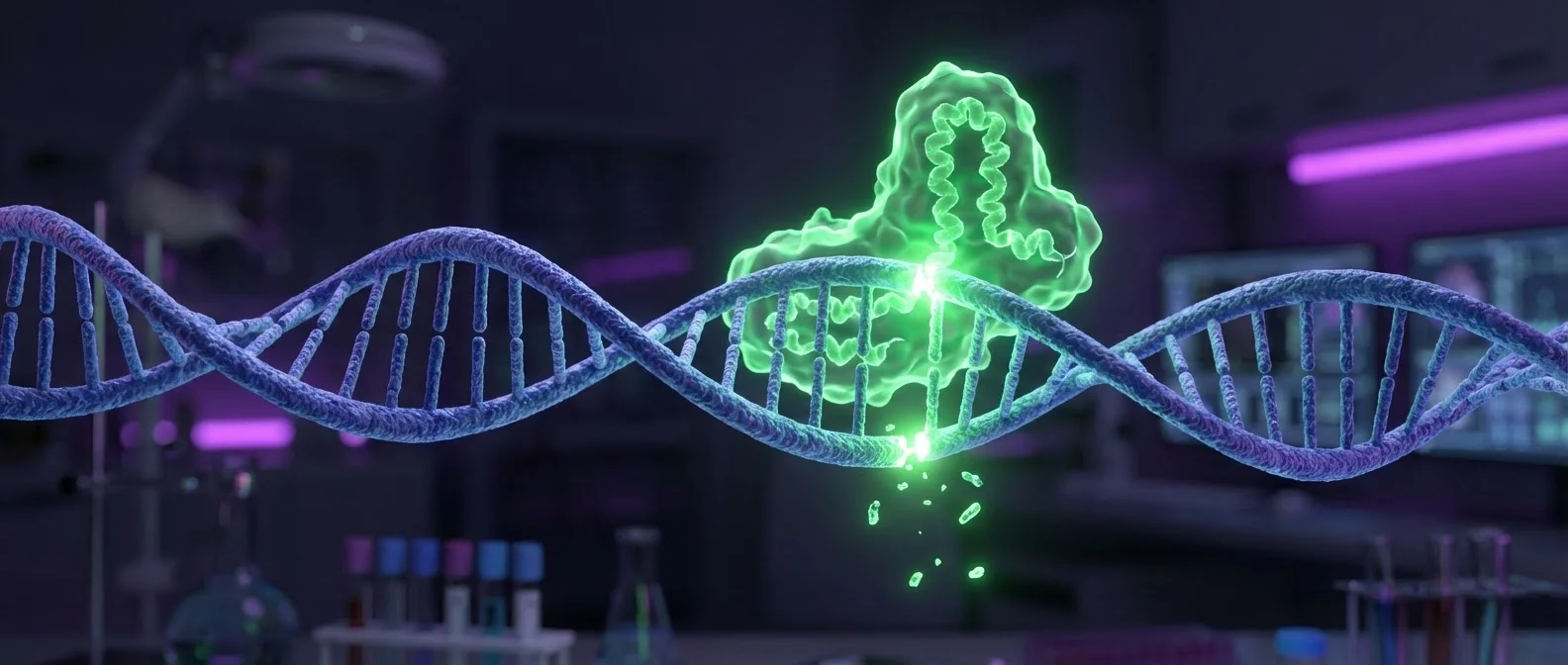
Το CRISPR (Clustered Regularly Interspaced Short Palindromic Repeats) είναι μια τεχνική γενετικής μηχανικής που επιτρέπει τροποποίηση του γονιδιώματος με πρωτοφανή ακρίβεια. Βασίζεται σε ένα φυσικό αμυντικό σύστημα βακτηρίων: το σύστημα CRISPR-Cas9, που τα βακτήρια χρησιμοποιούν για να καταστρέψουν ιούς.
Η πρωτεΐνη Cas9 λειτουργεί ως μοριακό «ψαλίδι». Σε συνδυασμό με ένα συνθετικό οδηγό RNA (gRNA), μπορεί να εντοπίσει μια συγκεκριμένη αλληλουχία DNA, να τη κόψει, και στη συνέχεια οι φυσικοί μηχανισμοί επιδιόρθωσης του κυττάρου «διορθώνουν» ή αντικαθιστούν τη βλάβη. Είναι ακριβές, οικονομικό και αποτελεσματικό — ποιότητες που παλαιότερες μέθοδοι (ZFNs, TALENs) δεν μπορούσαν να προσφέρουν.
Πώς λειτουργεί: Το οδηγό RNA εντοπίζει τον στόχο → Η Cas9 κόβει τη διπλή έλικα DNA → Οι κυτταρικοί μηχανισμοί επιδιορθώνουν ή αντικαθιστούν → Το γονίδιο διορθώνεται. Η ακρίβεια είναι τέτοια που μπορεί να στοχεύσει ένα γονίδιο ανάμεσα σε 3 δισεκατομμύρια ζεύγη βάσεων.
📖 Διαβάστε ακόμα: Zombie Κύτταρα: Πώς Επιστήμονες Αναστήνουν Νεκρά Βακτήρια
Η Ιστορία μιας Επανάστασης
Το 2012, οι Jennifer Doudna και Emmanuelle Charpentier δημοσίευσαν τη θεμελιώδη μελέτη που έδειξε ότι το CRISPR-Cas9 μπορεί να χρησιμοποιηθεί ως εργαλείο επεξεργασίας γονιδίων. Ένα χρόνο αργότερα, ο Feng Zhang εφάρμοσε το CRISPR σε ανθρώπινα κύτταρα στο εργαστήριο. Το 2015, το Science το ονόμασε «Ανακάλυψη της Χρονιάς». Ήδη Κινέζοι ερευνητές τροποποιούσαν μη βιώσιμα ανθρώπινα έμβρυα — προκαλώντας παγκόσμιο ηθικό σάλο.
Το 2016 ξεκίνησε η πρώτη κλινική δοκιμή σε ασθενείς με καρκίνο πνεύμονα στην Κίνα. Το 2018, ο He Jiankui ανακοίνωσε τα πρώτα γενετικά τροποποιημένα μωρά — καταδικάστηκε σε τρία χρόνια φυλάκιση. Το 2020, το Νόμπελ Χημείας δόθηκε στις Charpentier και Doudna — οι πρώτες δύο γυναίκες που μοιράστηκαν το βραβείο χωρίς αρσενικό συν-αποδέκτη.
Και τον Νοέμβριο του 2023, η πρώτη CRISPR θεραπεία εγκρίθηκε: το Casgevy.
📖 Διαβάστε ακόμα: Βιονικό Πάγκρεας: Το Τέλος του Διαβήτη;
Casgevy: Το Πρώτο Φάρμακο CRISPR
Τον Νοέμβριο 2023, η βρετανική ρυθμιστική αρχή MHRA ενέκρινε το Casgevy (exagamglogene autotemcel) — το πρώτο φάρμακο στον κόσμο βασισμένο στην τεχνολογία CRISPR-Cas9. Αναπτύχθηκε από τις Vertex Pharmaceuticals και CRISPR Therapeutics για δύο σοβαρές αιματολογικές παθήσεις: δρεπανοκυτταρική νόσο και βήτα-θαλασσαιμία.
Τα αποτελέσματα: 29 από 31 ασθενείς (93,5%) δεν χρειάστηκαν μετάγγιση αίματος για 12+ μήνες. Κανένας δεν παρουσίασε απόρριψη μοσχεύματος. Ακολούθησαν εγκρίσεις: Μπαχρέιν (Δεκέμβριος 2023), FDA (Δεκέμβριος 2023), Ευρωπαϊκή Ένωση (Φεβρουάριος 2024). Το κόστος: περίπου 2 εκατομμύρια ευρώ — μία δόση, αποτέλεσμα εφ" όρου ζωής.
"Υπάρχει τεράστια δύναμη στη γενετική μηχανική. Το ερώτημα δεν είναι αν μπορούμε, αλλά αν πρέπει."
— Jennifer Doudna, Νόμπελ Χημείας 2020Ασθένειες που Αλλάζει το CRISPR
Υπάρχουν περίπου 6.000 γνωστές γενετικές ασθένειες, οι περισσότερες ανίατες. Το CRISPR ανοίγει θεραπευτικές οδούς για πολλές:
Καρκίνος: Σε κλινικές δοκιμές, τροποποιημένα T-κύτταρα μέσω CRISPR καταστρέφουν καρκινικά κύτταρα. Τον Δεκέμβριο 2022, ένα 13χρονο κορίτσι θεραπεύτηκε από ανίατη T-κυτταρική λευχαιμία στο Great Ormond Street Hospital — η πρώτη τέτοια θεραπεία στον κόσμο.
HIV/AIDS: Το 2021, σε συνδυασμό αντιρετροϊκών και CRISPR εξαλείφθηκε ο ιός σε 9 από 23 ανθρωποποιημένα ποντίκια. Κλινικές δοκιμές του EBT-101 σε ανθρώπους ξεκίνησαν το 2022. Τον Μάρτιο 2024, ερευνητές του Πανεπιστημίου του Άμστερνταμ εξάλειψαν τον HIV σε κυτταρικές καλλιέργειες.
Νευρολογικές Παθήσεις: Alzheimer, Parkinson, μυϊκή δυστροφία Duchenne, σύνδρομο Dravet — το CRISPR δοκιμάζεται ως θεραπευτικό εργαλείο. Ο αιματοεγκεφαλικός φραγμός παραμένει πρόκληση, αλλά τα συστήματα μεταφοράς νανοσωματιδίων δείχνουν υποσχόμενα αποτελέσματα.
Καρδιαγγειακά & Τύφλωση: Η οικογενής υπερχοληστερολαιμία αντιμετωπίζεται μέσω τροποποίησης CRISPR του υποδοχέα LDLR. Για τη συγγενή αμαύρωση Leber, η Editas Medicine ξεκίνησε κλινικές δοκιμές το 2020 — με 20% σημαντική βελτίωση.
📖 Διαβάστε ακόμα: Επιγενωμική: Αλλαγή Γονιδίων Χωρίς Αλλαγή DNA
Prime Editing: Η Επόμενη Γενιά
Ενώ το κλασικό CRISPR-Cas9 κόβει τη διπλή έλικα DNA (με κίνδυνο σφαλμάτων), το Prime Editing εισάγει τροποποιήσεις χωρίς να κόψει και τους δύο κλώνους. Ο David Liu (MIT) ανέπτυξε αυτή τη μέθοδο που μπορεί θεωρητικά να διορθώσει το 89% των γνωστών γενετικών ελαττωμάτων.
Παράλληλα, η τεχνική PASTE (2022) επιτρέπει εισαγωγή τεράστιων τμημάτων DNA — έως 36.000 ζεύγη βάσεων — χωρίς προβληματικές πανφωτικές θραύσεις, ανοίγοντας δρόμο για θεραπεία νοσημάτων πολλαπλών μεταλλάξεων.
CRISPR ως διαγνωστικό εργαλείο: Πέραν της θεραπείας, το CRISPR χρησιμοποιείται και στη διαγνωστική. Τα συστήματα SHERLOCK και AIOD-CRISPR ανιχνεύουν ιούς (συμπεριλαμβανομένου του SARS-CoV-2) με ακρίβεια έως 10 αντίγραφα ανά μικρολίτρο — σε φορητές, οικονομικές συσκευές.
CRISPR στη Γεωργία
Η επανάσταση δεν περιορίζεται στην ιατρική. Τον Σεπτέμβριο 2021, τα πρώτα τρόφιμα CRISPR πωλήθηκαν στην Ιαπωνία — ντομάτες με 5 φορές περισσότερο GABA, ένα ηρεμιστικό αμινοξύ. Ακολούθησαν ψάρια που μεγαλώνουν στο διπλάσιο μέγεθος.
Η τεχνολογία εφαρμόζεται σε ρύζι, σιτάρι, σόγια, κακάο — για αυξημένη απόδοση, αντοχή σε ασθένειες, μειωμένα αλλεργιογόνα (σιτάρι χωρίς γλουτένη), βελτιωμένη θρεπτική αξία και παρατεταμένη διάρκεια ζωής.
📖 Διαβάστε ακόμα: Μίνι Εγκέφαλοι σε Chip: Λύνουν Προβλήματα Μηχανικής
Ηθικά Διλήμματα και Κίνδυνοι
Off-target effects: Το CRISPR μπορεί να «κόψει» λάθος σημεία στο DNA. Νεότερες εκδόσεις (Cas9 nickases, base editors) μειώνουν σημαντικά αυτόν τον κίνδυνο.
Τροποποίηση αναπαραγωγικής σειράς: Η τροποποίηση ανθρώπινων εμβρύων (germline editing) κληρονομείται στις επόμενες γενιές. Η υπόθεση He Jiankui (2018) αποδεικνύει τους κινδύνους.
Πρόσβαση και κόστος: Με κόστος ~2 εκατ. € ανά θεραπεία, ποιος θα έχει πρόσβαση; Η ανισότητα στην υγεία μπορεί να βαθύνει, δημιουργώντας «γενετικά πλούσιους» και «γενετικά φτωχούς».
Βιοηθική και ευγονική: Αν μπορούμε να «διορθώσουμε» ασθένειες, μπορούμε να «βελτιώσουμε» χαρακτηριστικά; Η γραμμή μεταξύ θεραπείας και ευγονικής γίνεται ολοένα πιο θολή.
Τι Μας Περιμένει
Η τεχνολογία CRISPR εξελίσσεται με ρυθμό που ξεπερνά κάθε πρόβλεψη. Νέες εκδόσεις (Cas12, Cas13, base editing, prime editing) επεκτείνουν τις δυνατότητες σε επεξεργασία RNA, επιγενωμική, αγροτεχνολογία και βιοασφάλεια. Οι κλινικές δοκιμές πολλαπλασιάζονται — πάνω από 80 ήταν σε εξέλιξη το 2024.
Μέχρι το 2030, αναλυτές προβλέπουν θεραπείες CRISPR για μυϊκή δυστροφία, κυστική ίνωση, νόσο Huntington και ορισμένους καρκίνους. Μέχρι το 2040, η γονιδιακή θεραπεία θα μπορούσε να γίνει τόσο ρουτίνα όσο τα αντιβιοτικά σήμερα.
Η πραγματική πρόκληση δεν είναι πλέον τεχνολογική — είναι κοινωνική, ηθική και οικονομική. Αν μπορέσουμε να εξαλείψουμε τις κληρονομικές ασθένειες, σε ποιον ανήκει αυτό το δώρο; Η απάντηση θα καθορίσει αν το CRISPR γίνει η μεγαλύτερη ιατρική επανάσταση — ή ο μεγαλύτερος μοχλός ανισότητας.