Ο λόγος που δεν προσομοιώνουμε ακριβώς μόρια στους κλασικούς υπολογιστές είναι ότι κάνουν κβαντικούς υπολογισμούς. Τι αλλάζει όταν χρησιμοποιούμε κβαντικό hardware;
📖 Διαβάστε περισσότερα: Κβαντική προσομοίωση υλικών: Ο δρόμος στον υπεραγωγό
🧪 Γιατί οι κλασικοί υπολογιστές δεν μπορούν να «δουν» τα μόρια
Η χημεία, στη βάση της, είναι κβαντική φυσική. Κάθε μόριο αποτελείται από πυρήνες και ηλεκτρόνια που υπακούν στην εξίσωση Schrödinger. Αλλά η ακριβής επίλυσή της δεν είναι εφικτή παρά μόνο για το απλούστερο σύστημα — το μεμονωμένο άτομο υδρογόνου. Μόλις προστεθεί ένα δεύτερο ηλεκτρόνιο, η πολυπλοκότητα εκρήγνυται.
Ο λόγος είναι ο χώρος Hilbert: ο μαθηματικός «χώρος» όπου ζει η κυματοσυνάρτηση ενός κβαντικού συστήματος αυξάνεται εκθετικά με τον αριθμό σωματιδίων. Σύμφωνα με εκτιμήσεις, ένα σύστημα μόλις 30 σωματιδίων απαιτεί τόσους πόρους μνήμης που ακόμα και οι ισχυρότεροι υπερυπολογιστές αδυνατούν να τους χειριστούν. Για ένα φαρμακευτικό μόριο με εκατοντάδες ηλεκτρόνια, η κατάσταση είναι αδιέξοδη.
Η κλασική υπολογιστική χημεία αντιμετωπίζει αυτό το πρόβλημα μέσω προσεγγίσεων. Η μέθοδος Hartree-Fock, που αναπτύχθηκε στο MIT τη δεκαετία του 1950, αντιμετωπίζει κάθε ηλεκτρόνιο σαν να κινείται μέσα σε ένα μέσο πεδίο — αγνοώντας τη λεπτομερή αλληλεπίδραση μεταξύ ηλεκτρονίων. Η θεωρία συναρτησιακού πυκνότητας (Density Functional Theory, DFT), που κέρδισε το Νόμπελ Χημείας 1998 για τους Walter Kohn και John Pople, κλιμακώνεται τυπικά ως O(N³). Αλλά η πιο ακριβής μέθοδος, CCSD(T), κλιμακώνεται ως O(M⁷), περιορίζοντας τη χρήση της σε μόρια με λιγότερα από 25 άτομα.
Δεν μας λείπει η θεωρία — μας λείπει η υπολογιστική ισχύς να την εφαρμόσουμε σε πολύπλοκα μόρια.
💡 Η ιδέα του Feynman: «Χρησιμοποιήστε κβαντικά συστήματα»
Η ιδέα ότι η φύση «τρέχει» κβαντικούς υπολογισμούς δεν είναι νέα. Ο Yuri Manin τη διατύπωσε πρώτος το 1980 στο βιβλίο Computable and Noncomputable, και ο Richard Feynman ανεξάρτητα το 1982 στο κομβικό άρθρο «Simulating Physics with Computers» στο International Journal of Theoretical Physics. Η λογική τους ήταν απλή: αν η φύση λειτουργεί κβαντικά, τότε μόνο ένα κβαντικό σύστημα μπορεί να την προσομοιώσει αποδοτικά.
Ο Seth Lloyd απέδειξε θεωρητικά το 1996 στο Science ότι ένας «καθολικός κβαντικός προσομοιωτής» μπορεί να αναπαράξει την εξέλιξη οποιουδήποτε κβαντικού συστήματος χρησιμοποιώντας αριθμό qubits ανάλογο του αριθμού σωματιδίων — αντί για τον εκθετικό αριθμό bits που απαιτεί ένας κλασικός υπολογιστής. Αυτό ήταν θεωρητικά επαναστατικό, αλλά η πρακτική υλοποίηση απαιτούσε δεκαετίες.
⚙️ Πώς λειτουργεί η κβαντική χημική προσομοίωση
Η βασική ιδέα είναι εξαιρετικά κομψή. Αντί να αναπαριστούμε τα ηλεκτρόνια ενός μορίου ως αριθμούς σε κλασική μνήμη (bits), τα «χαρτογραφούμε» σε qubits — κβαντικά bits που μπορούν να βρίσκονται σε υπέρθεση και να εμπλέκονται μεταξύ τους. Οι μαθηματικοί μετασχηματισμοί Jordan-Wigner ή Bravyi-Kitaev μετατρέπουν τον Hamiltonian ενός μορίου σε γινόμενα τανυστών πινάκων Pauli, εκφράσεις που μπορεί να «τρέξει» ένα κβαντικό κύκλωμα.
Ο πιο δημοφιλής αλγόριθμος σήμερα είναι ο Variational Quantum Eigensolver (VQE), που προτάθηκε το 2014 από τους Alberto Peruzzo, Alán Aspuru-Guzik και Jeremy O'Brien. Ο VQE είναι υβριδικός: ένας κβαντικός επεξεργαστής προετοιμάζει μια δοκιμαστική κυματοσυνάρτηση (ansatz) και μετρά την ενέργειά της, ενώ ένας κλασικός υπολογιστής βελτιστοποιεί τις παραμέτρους μέσω gradient descent. Η διαδικασία επαναλαμβάνεται μέχρι να βρεθεί η θεμελιώδης κατάσταση — η κατάσταση ελάχιστης ενέργειας του μορίου.
• 2014: Πρώτη προσομοίωση HeH⁺ (υδρίδιο του ηλίου) σε φωτονικό κβαντικό επεξεργαστή
• 2017: Η ομάδα Kandala (IBM) προσομοιώνει BeH₂ (υδρίδιο βηρυλλίου) με hardware-efficient VQE
• 2020: Η Google χρησιμοποιεί τον Sycamore (12 qubits) για Hartree-Fock προσομοίωση αλυσίδας H₁₂
📖 Διαβάστε περισσότερα: Κβαντικοί υπολογιστές: Η νέα ελπίδα κατά της κλιματικής
💊 Από τα μικρά μόρια στα φάρμακα
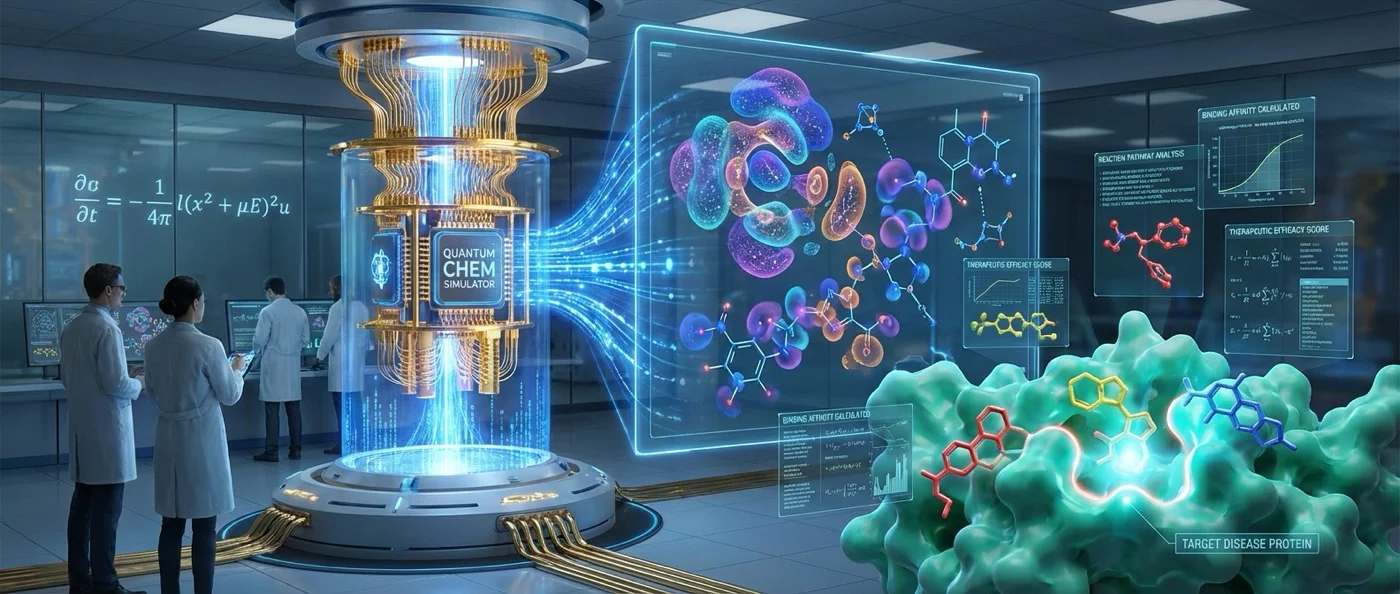
Η υπόσχεση είναι τεράστια. Σήμερα η ανάπτυξη ενός νέου φαρμάκου κοστίζει κατά μέσον όρο 2,6 δισεκατομμύρια δολάρια και διαρκεί 10-15 χρόνια. Ένα μεγάλο μέρος αυτού του κόστους αφιερώνεται στον πειραματικό έλεγχο μορίων-υποψηφίων που τελικά αποτυγχάνουν. Αν μπορούσαμε να προσομοιώσουμε ακριβώς πώς ένα μόριο αλληλεπιδρά με μια πρωτεΐνη-στόχο, θα εξαλείφαμε αναρίθμητα αδιέξοδα.
Η υπολογιστική χημεία ήδη χρησιμοποιείται εκτεταμένα στη φαρμακευτική βιομηχανία. Βάσεις δεδομένων όπως η ChEMBL και η DrugBank αποθηκεύουν εκατομμύρια πειραματικά δεδομένα, ενώ μέθοδοι DFT χρησιμοποιούνται καθημερινά για να υπολογίσουν ενέργειες HOMO/LUMO και μοριακά τροχιακά υποψήφιων φαρμάκων. Αλλά η ακρίβεια αυτών των μεθόδων παραμένει περιορισμένη — η «χημική ακρίβεια» (1 kcal/mol ή 4 kJ/mol) που χρειάζεται για ρεαλιστικές προβλέψεις συχνά δεν επιτυγχάνεται σε μεγάλα μόρια.
Ένας «ιερός γρίφος» εδώ είναι το FeMoco — ο σιδηρο-μολυβδαινικός πυρήνας του ενζύμου νιτρογενάση, που καταλύει τη δέσμευση ατμοσφαιρικού αζώτου σε αμμωνία. Η βιομηχανική σύνθεση αμμωνίας (διεργασία Haber-Bosch) καταναλώνει 1-2% της παγκόσμιας ενέργειας. Αν κατανοήσουμε πώς η νιτρογενάση τα καταφέρνει σε θερμοκρασία δωματίου, θα μπορέσουμε να σχεδιάσουμε καταλύτες που εξοικονομούν τεράστια ποσά ενέργειας. Αλλά το FeMoco περιέχει σύμπλεγμα μετάλλων μετάπτωσης — ακριβώς το είδος συστημάτων όπου οι κλασικές μέθοδοι αδυνατούν.
⚖️ Η μεγάλη αμφισβήτηση: είμαστε αρκετά κοντά;
Εδώ βρίσκεται η πραγματική ένταση στον τομέα. Οι σημερινοί κβαντικοί υπολογιστές ανήκουν στην εποχή NISQ (Noisy Intermediate-Scale Quantum) — διαθέτουν δεκάδες ή εκατοντάδες qubits, αλλά με σημαντικό θόρυβο και σφάλματα. Ο VQE, αν και θεωρητικά υπόσχεται πολλά, αντιμετωπίζει σοβαρά πρακτικά εμπόδια.
Ένα κεντρικό πρόβλημα είναι τα «barren plateaus» (άγονα οροπέδια): καθώς αυξάνεται ο αριθμός qubits, η κλίση της συνάρτησης κόστους τείνει στο μηδέν, κάνοντας τη βελτιστοποίηση εξαιρετικά δύσκολη. Ο αλγόριθμος μπορεί να κολλήσει σε μη βέλτιστες λύσεις χωρίς να «βλέπει» πού βρίσκεται η πραγματική θεμελιώδης κατάσταση.
Από την άλλη, οι υποστηρικτές τονίζουν ότι η πρόοδος είναι εκθετική. Το 2014 η καλύτερη επίδειξη ήταν ένα μόριο δύο ατόμων (HeH⁺). Σε μόλις έξι χρόνια, η Google προσομοίωσε αλυσίδα 12 ατόμων υδρογόνου. Η ανάπτυξη τεχνικών αντιμετώπισης σφαλμάτων (error mitigation), σε συνδυασμό με τη μείωση θορύβου στα qubits, υπόσχεται χημικά σχετικές προσομοιώσεις εντός της επόμενης δεκαετίας.
Η κβαντική χημεία δεν θα αντικαταστήσει αύριο τα εργαστήρια. Αλλά ενδέχεται να αλλάξει ριζικά τον τρόπο που ανακαλύπτουμε φάρμακα — αν ξεπεράσουμε τα τεχνολογικά εμπόδια.
Τα Νόμπελ Χημείας 2013 (Martin Karplus, Michael Levitt, Arieh Warshel) αναγνώρισαν πολύκλιμακα μοντέλα που συνδυάζουν κβαντική μηχανική με κλασική μηχανική (QM/MM) για μεγάλα βιομοριακά συστήματα. Η κβαντική υπολογιστική χημεία αντιπροσωπεύει το επόμενο βήμα: αποκλειστικά κβαντικές μεθόδους χωρίς κλασικές προσεγγίσεις στο χημικό μέρος.
Η σύγκρουση απόψεων παραμένει ανοιχτή. Ορισμένοι ακαδημαϊκοί θεωρούν ότι η φαρμακευτική εφαρμογή απέχει δεκαετίες — οι κβαντικοί υπολογιστές πρέπει πρώτα να αποδείξουν «κβαντικό πλεονέκτημα» σε χημικά προβλήματα που δεν μπορεί να λύσει ο καλύτερος κλασικός αλγόριθμος. Άλλοι πιστεύουν ότι ακόμα και η σημερινή NISQ τεχνολογία μπορεί να παρέχει χρήσιμα αποτελέσματα σε στοχευμένα προβλήματα, ανοίγοντας τον δρόμο για φαρμακευτικές ανακαλύψεις που σήμερα φαίνονται αδύνατες.