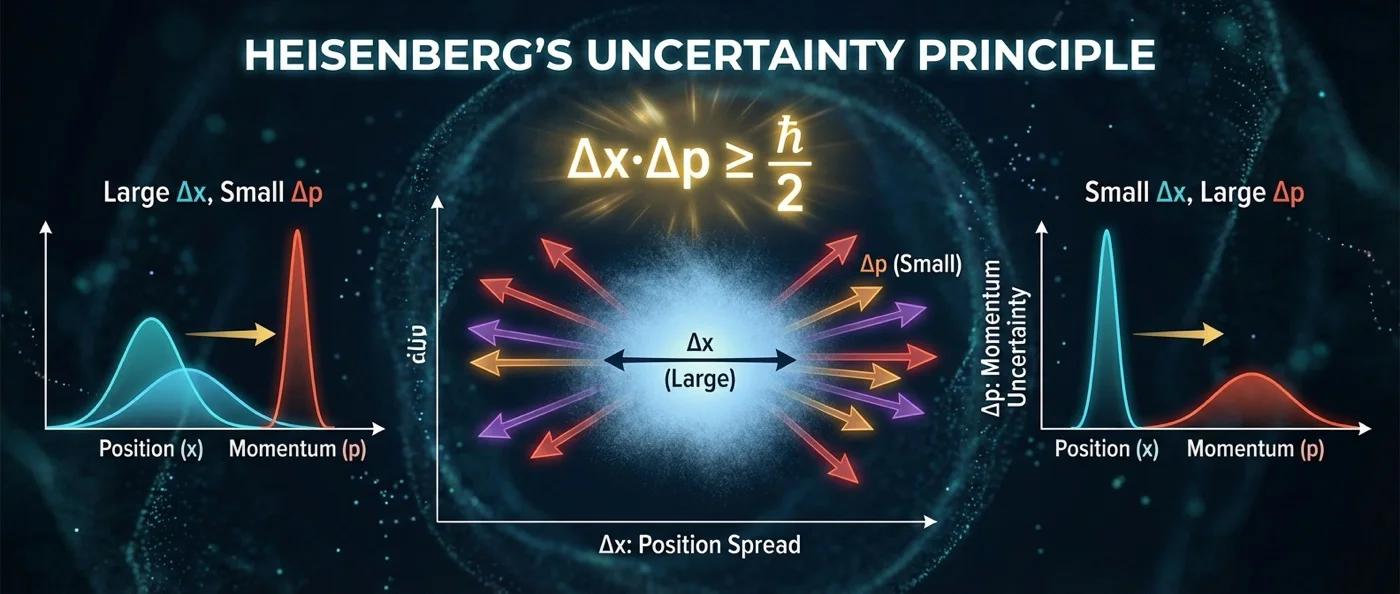
Δεν υπάρχει τρόπος να γνωρίζουμε ταυτόχρονα τη θέση και ορμή ενός σωματιδίου. Αυτό δεν είναι τεχνολογικό εμπόδιο — είναι θεμελιώδης νόμος της φύσης.
🌐 Ένας περίεργος κόσμος με ενσωματωμένα όρια
Φαίνεται σαν τεχνικό πρόβλημα. Σαν να λέμε: «δεν έχουμε αρκετά ακριβή όργανα». Αλλά η αρχή αβεβαιότητας του Χάιζενμπεργκ λέει κάτι πολύ πιο ριζοσπαστικό. Λέει ότι η φύση η ίδια δεν έχει ταυτόχρονα ακριβή θέση ΚΑΙ ακριβή ορμή για ένα σωματίδιο. Δεν είναι ότι δεν μπορούμε να μετρήσουμε — είναι ότι δεν υπάρχει τίποτα εκεί να μετρηθεί ταυτόχρονα.
Αυτό είναι ίσως το πιο ανατρεπτικό μήνυμα της κβαντικής μηχανικής. Και σίγουρα αυτό που δυσκολεύτηκε περισσότερο ο κόσμος να δεχτεί — ακόμα και φυσικοί του διαμετρήματος του Αϊνστάιν.
🏝️ Ο νεαρός φυσικός στο νησί Χέλγκολαντ
Τον Ιούνιο του 1925, ο 23χρονος Βέρνερ Χάιζενμπεργκ κατέφυγε στο νησί Χέλγκολαντ στη Βόρεια Θάλασσα, μακριά από τη γύρη που επιδείνωνε τον αλλεργικό πυρετό του. Εκεί, ανάμεσα σε αναρριχήσεις στους βράχους και απομνημόνευση ποιημάτων του Γκαίτε, έκανε μια ανακάλυψη που θα άλλαζε τη φυσική για πάντα.
Αργά το βράδυ, στις τρεις τα ξημερώματα, ολοκλήρωσε υπολογισμούς που έδειχναν πως τα κβαντικά μεγέθη δεν αντιμετατίθενται — η σειρά με την οποία μετράς θέση και ορμή μετράει. Ήταν τόσο συγκλονισμένος που δεν μπόρεσε να κοιμηθεί. Περίμενε την ανατολή του ήλιου στην κορυφή ενός βράχου.
Αυτό το paper, το περίφημο Umdeutung (Αναδιατύπωση), δημοσιεύτηκε τον Σεπτέμβριο του 1925 και μαζί με τους Max Born και Pascual Jordan θεμελίωσε τη μηχανική πινάκων — την πρώτη αυστηρή μαθηματική διατύπωση της κβαντικής μηχανικής. Η κεντρική ιδέα ήταν απλή αλλά επαναστατική: η θέση X και η ορμή P δεν είναι αριθμοί αλλά πίνακες, και η σειρά πολλαπλασιασμού τους έχει σημασία. Μαθηματικά: XP − PX = iℏ, όπου ℏ η ανηγμένη σταθερά Planck.
📐 Ο τύπος που άλλαξε τη φιλοσοφία
Τον Φεβρουάριο του 1927, ο Χάιζενμπεργκ έγραψε στον Wolfgang Pauli ένα γράμμα όπου περιέγραφε για πρώτη φορά αυτό που σήμερα ονομάζουμε αρχή αβεβαιότητας. Στο ιστορικό paper «Über den anschaulichen Inhalt der quantentheoretischen Kinematik und Mechanik» (Για το εποπτικό περιεχόμενο της κβαντοθεωρητικής κινηματικής και μηχανικής), ο ίδιος χρησιμοποίησε τον όρο «Ungenauigkeit» (ανακρίβεια). Μόνο στην υποσημείωση εμφανίστηκε η λέξη «Unsicherheit» (αβεβαιότητα) — κι αργότερα χρησιμοποιούσε πάντα «Unbestimmtheit» (απροσδιοριστία).
Η αυστηρή μαθηματική ανισότητα αποδείχθηκε τον ίδιο χρόνο (1927) από τον Earle Hesse Kennard:
Η τυπική απόκλιση της θέσης (σx) πολλαπλασιασμένη με την τυπική απόκλιση της ορμής (σp) δεν μπορεί ποτέ να πέσει κάτω από ℏ/2. Όσο πιο ακριβώς γνωρίζεις τη θέση, τόσο πιο αβέβαιη γίνεται η ορμή — και αντίστροφα. Δεν υπάρχει τρόπος να «ξεγελάσεις» αυτό τον περιορισμό.
🔍 Γιατί ΔΕΝ φταίει η μέτρηση
Μια διαδεδομένη παρεξήγηση είναι ότι η αβεβαιότητα οφείλεται στο ότι η μέτρηση «ενοχλεί» το σωματίδιο. Αυτό είναι το λεγόμενο observer effect, αλλά δεν είναι η αρχή αβεβαιότητας.
Ο ίδιος ο Χάιζενμπεργκ αρχικά χρησιμοποίησε ένα νοητικό πείραμα — ένα μικροσκόπιο ακτίνων γάμμα — για να εξηγήσει την αρχή. Αν ρίξεις ένα φωτόνιο μικρού μήκους κύματος σε ένα ηλεκτρόνιο, μπορείς να μετρήσεις ακριβώς τη θέση του. Αλλά το φωτόνιο μεταφέρει τεράστια ορμή και «σπρώχνει» το ηλεκτρόνιο με αβέβαιο τρόπο. Αντίστροφα, ένα φωτόνιο μεγάλου μήκους κύματος δεν ενοχλεί πολύ την ορμή, αλλά δεν αποκαλύπτει με ακρίβεια τη θέση.
Ωστόσο, ο Niels Bohr έδειξε ότι αυτή η εξήγηση δεν ήταν πλήρως ακριβής. Η αβεβαιότητα είναι εγγενής ιδιότητα κάθε κυματικού συστήματος. Μια κυματοσυνάρτηση στενά εντοπισμένη στο χώρο αντιστοιχεί αναγκαστικά σε ευρεία κατανομή στο χώρο ορμής μέσω του μετασχηματισμού Fourier — και αντίστροφα. Αυτό δεν έχει καμία σχέση με τα όργανα μέτρησης. Είναι μαθηματική αναγκαιότητα.
⏱️ Αβεβαιότητα ενέργειας-χρόνου
Η αρχή δεν περιορίζεται στο ζεύγος θέση-ορμή. Υπάρχει ανάλογη σχέση για ενέργεια-χρόνο, αν και η ακριβής διατύπωσή της είναι πιο λεπτή. Το 1945, οι Leonid Mandelstam και Igor Tamm απέδειξαν ότι η διάρκεια μιας ενεργειακής μέτρησης σχετίζεται με την ακρίβειά της: ΔΕ · Δt ≥ ℏ/2.
Αυτό εξηγεί γιατί τα ασταθή σωματίδια, όπως το σωματίδιο Δέλτα (Δ), που ζουν μόλις 10−23 δευτερόλεπτα, έχουν ευρεία κατανομή μάζας: ±120 MeV/c² γύρω από τα 1.232 MeV/c². Η σύντομη ζωή τους αντανακλάται σε μεγαλύτερη ενεργειακή αβεβαιότητα.
🎲 «Ο Θεός δεν παίζει ζάρια» — η μεγάλη αντίρρηση
Ο Αϊνστάιν δεν δέχθηκε ποτέ ότι η αβεβαιότητα είναι θεμελιώδης. Πίστευε ότι η τυχαιότητα αντανακλά την άγνοιά μας, όχι τη φύση της πραγματικότητας. Στο ιστορικό paper EPR (Einstein-Podolsky-Rosen, 1935), υποστήριξε ότι η κβαντική μηχανική είναι «ελλιπής» — ότι πρέπει να υπάρχουν κρυφές μεταβλητές που καθορίζουν ταυτόχρονα θέση και ορμή.
Η Ερμηνεία της Κοπεγχάγης, που υποστήριξαν ο Bohr και ο Χάιζενμπεργκ, απαντούσε: δεν υπάρχει θεμελιώδης πραγματικότητα πέρα από αυτό που μπορούμε να μετρήσουμε. Η κβαντική κατάσταση δεν περιγράφει κάποιο «πραγματικό» αντικείμενο, αλλά αποτελεί εργαλείο πρόβλεψης πειραματικών αποτελεσμάτων.
Ο ίδιος ο Χάιζενμπεργκ ήταν ξεκάθαρος: δεν μπορούμε ποτέ να γνωρίζουμε τι «πραγματικά είναι» ένα σωματίδιο. Μπορούμε μόνο να γνωρίζουμε αριθμούς σε πίνακες που περιγράφουν κάτι γι' αυτά.
💡 Τι σημαίνει για εμάς
Η αρχή αβεβαιότητας δεν είναι σημαντική μόνο φιλοσοφικά. Σήμερα, η κβαντική κρυπτογραφία βασίζεται ακριβώς σε αυτήν: κάθε απόπειρα υποκλοπής αλλάζει αναγκαστικά τη μέτρηση, γιατί η αβεβαιότητα δεν επιτρέπει πλήρη γνώση χωρίς διαταραχή. Οι κβαντικοί υπολογιστές λειτουργούν ακριβώς μέσα σε αυτό το πλαίσιο αβεβαιότητας — εκμεταλλευόμενοι την υπέρθεση αντί να τη φοβούνται.
Ο Χάιζενμπεργκ κέρδισε το Νόμπελ Φυσικής το 1932 «για τη δημιουργία της κβαντικής μηχανικής». Αργότερα, αισθάνθηκε ότι οι Born και Jordan δεν αναγνωρίστηκαν αρκετά. Σε γράμμα στον Born, παραδέχθηκε «κακή συνείδηση» που πήρε μόνος του το βραβείο. Ο Born πήρε τελικά το δικό του Νόμπελ το 1954 — για τη στατιστική ερμηνεία της κυματοσυνάρτησης.
🌌 Η φύση ορίζει τα δικά της σύνορα
Η αρχή αβεβαιότητας μας θυμίζει κάτι βαθύ: ο κόσμος δεν μας χρωστάει διαφάνεια. Δεν φτιάχτηκε για να κατανοηθεί πλήρως. Υπάρχουν όρια στη γνώση που δεν είναι αποτέλεσμα ανθρώπινης αδυναμίας, αλλά αρχιτεκτονικά στοιχεία της ίδιας της πραγματικότητας.
Σχεδόν 100 χρόνια μετά το γράμμα του Χάιζενμπεργκ στον Pauli, η αρχή αβεβαιότητας παραμένει αθίκτη. Κανένα πείραμα δεν την έχει παραβιάσει. Κάθε απόπειρα ταυτόχρονης ακριβούς μέτρησης θέσης και ορμής αποτυγχάνει — όχι λόγω πειραματικών περιορισμών αλλά θεμελιακά. Ο κόσμος, στο βαθύτερο επίπεδό του, διατηρεί μια αναφαίρετη αδιαφάνεια. Κι ίσως αυτό να είναι το πιο σημαντικό που μας δίδαξε η κβαντική φυσική.